近年来,难治的胃肠道肿瘤已成为业内聚焦的热点, 也是本次CSCO大会重点讨论的内容之一。其中,ATTRACTION-2试验作为针对亚洲晚期转移性胃癌患者的免疫治疗“开拓性”研究,因其2年生存率提高3倍的结果而备受关注。今年大会更就该研究的中国台湾地区亚组数据分析报告进行了专题探讨。基于此项研究结果,今日肿瘤特别邀请了浙江大学医学院附属邵逸夫医院副院长潘宏铭教授为我们做深度解读,并进一步阐释胃肠道癌症相关诊疗进展。
ATTRACTION-2研究中国台湾人群数据亮点荟萃:
中国台湾地区亚组分析的疗效(客观缓解率为12.5%,完全缓解率达4.2%)和安全性结果与ATTRACTION-2研究整体人群数据基本一致。
与安慰剂相比,纳武利尤单抗组总生存期风险比为0.49,降低一半以上的死亡风险;显著生存获益强化了纳武利尤单抗用于三线以上晚期胃癌治疗的附加价值。
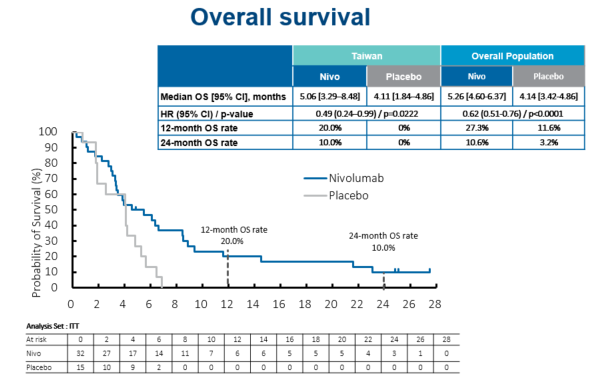
纳武利尤单抗组12个月总生存率为20%,24个月总生存率为10%。
纳武利尤单抗组中位总生存期为5.06个月,安慰剂组为4.11个月。
潘宏铭教授表示,在今年4月CSCO胃癌诊疗指南对PD-1抑制剂推荐等级升级的背景下,基于该研究结果,希望用于胃癌三线治疗的免疫治疗药物能够尽快获批,让更多患者尽早获益。
数说ATTRACTION-2研究,免疫疗法打响亚洲保“胃”战
回顾经典,探路初胜利
2014年,多中心Ⅲ期临床试验ATTRACTION-2成为全球首个开启的晚期胃癌免疫治疗探索,研究的主体目标人群为亚洲胃癌患者。
ATTRACTION-2研究共纳入493例来自日本、韩国与中国台湾的患者,旨在评估纳武利尤单抗(Nivolumab)治疗不可切除、经治晚期或复发性胃及胃食管交界处癌的有效性及安全性。
1年随访数据显示,纳武利尤单抗可使死亡风险显著降低37%,且纳武利尤单抗组总生存(OS)率显著高于安慰剂组,分别为26.2%和10.9%。纳武利尤单抗在胃癌中的安全性亦与既往的实体瘤研究类似,治疗相关不良事件(TRAE)所致的停药率与安慰剂组相似。
基于ATTRACTION-2研究的“希望性”成果,2017年,纳武利尤单抗成为全球首个获批用于治疗不可切除晚期或复发性胃癌的免疫治疗药物。
长久获益,中国不缺席
2年的延长随访发现,纳武利尤单抗组与安慰剂组2年OS率分别达到10.6%和3.2%;在纳武利尤单抗组中,出现了3例CR患者,在获得肿瘤缓解患者(CR+PR)中已观察到最大生存获益 —— 中位OS达 26.6个月,1年OS率为87.1%,2年OS率为61.3%;且在随访过程中未发现新的TRAE。
由此,更长久的随访结果进一步证明,纳武利尤单抗能显著提高不可切除晚期或复发性胃癌的总生存,2年OS率较安慰剂组提高超过3倍,对于CR或PR的患者能够显示出更高的有效率。
而根据CSCO大会上ATTRACTION-2研究针对入组的10%中国台湾患者报告情况,纳武利尤单抗同样能为中国晚期胃癌患者带来卓越的生存获益。
在中国台湾患者中,纳武利尤单抗组1年OS率为20%,2年OS率为10%,而安慰剂组则均已为0%;更值得注意的是,纳武利尤单抗组的2年中位OS也显著优于安慰剂组(5.06个月 vs 4.11个月,HR=0.49,95%CI 0.24-0.99,P=0.0222)。
同时,在中国台湾地区亚组患者中,纳武利尤单抗的客观缓解率(ORR)达到12.5%,包含了4.2%的CR患者比率;疾病控制率(DCR)亦与整体人群大体一致。此外,该亚组患者的肿瘤负荷减少比例近一半,安全性结果良好,与整体人群情况基本符合,没有新的针对中国亚组的TRAE发现。
始出东方力创全球突破,因地制宜尽显中国特色
受到饮食习惯影响,中国已经成为胃癌“重灾区”,五年生存率为仅为30%左右。究其原因,其一是大多数患者就诊时已为疾病晚期;其二,对于晚期胃癌的治疗,医生手中缺乏有效的“武器”;其三,胃癌具有高度的异质性和复杂的肿瘤微环境,治疗的有效靶点屈指可数,加之空腔脏器等因素共同作用,给精准治疗带来了巨大的难度;其四,胃癌治疗后易复发及转移,而在一线二线治疗之后,后线(三线及以上)几乎没有合适的药物,治疗需求远未被满足,令医生倍感掣肘。
长久以来,医疗尖端科研成果往往出自西方,许多“不治之症”在现代医疗技术发展之下也出现了利好转变,而胃癌是项例外。纵观全球,约75%的胃癌发病率与死亡率来自亚洲,特别高发于中、日、韩三国,且由于异质性影响,东方多发的远端胃癌与西方近端胃癌具有明显不同;故解决全球胃癌的最大难题,还需从“胃癌大国”实情出发,针对问题,打破瓶颈。
ATTRACTION-2研究便是破局者,其开创性地由亚洲人群入手,使最为迫切寻求全新治疗方案的胃癌患者率先看到了曙光。继ATTRACTION-2研究之后,多项胃癌免疫治疗的临床研究也陆续在亚洲以及全球更多中心开展,展示了免疫治疗在胃癌治疗领域的巨大潜力,也成就了前沿医疗自东方至西方的突破性发展之路。
面对我国大批晚期胃癌患者的实际需求,基于ATTRACTION-2领衔的免疫治疗研究结果,PD-1单抗第一时间被纳入2018年《CSCO原发性胃癌诊疗指南》,以单药用于晚期胃癌的三线治疗,推荐级别为Ⅲ级;今年更新版指南对免疫治疗的推荐级别由Ⅲ级提升为Ⅱ级,证据级别改为1B类,进一步奠定了免疫治疗在晚期胃癌后线治疗中的重要地位。
本次汇报的中国台湾地区亚组数据,于中国大陆的胃癌患者而言,相比日本韩国数据更具借鉴意义。一方面,中国台湾的人种与中国大陆的人种同种同根、血浓于水,研究数据针对同一个种族的应用更为适合;另一方面,胃癌发病率与死亡率有明显的地域差别,关系到地域环境、饮食习惯、经济水平等因素,中国台湾与中国大陆的疾病情况也更为相似。
据统计,胃癌患者就诊即晚期的比率在中国台湾约为60%,初诊中晚期情况在中国大陆达80%,早筛率与日本韩国尚有距离;且中国台湾与中国大陆的晚期胃癌或胃食管连接癌(AGC)通常均与预后不良有关。因此,ATTRACTION-2研究的中国台湾地区亚组生存获益情况将为中国大批胃癌患者带来更多长期生存的期待。
结直肠癌深陷晚期困境,免疫联合推进前线探索
在我国,多数结直肠癌患者在发现时已属于中晚期,治疗较为困难,其中还有约6.5%的转移性结直肠癌患者因带有微卫星高度不稳定(MSI-H)或错配修复基因缺陷(dMMR)突变而更加难以受益于传统治疗手段,预后较差。
2017年,美国FDA批准纳武利尤单抗用于MSI-H/dMMR型转移性结直肠癌的治疗,开启了结直肠癌免疫治疗的新时代。2019年新版《CSCO结直肠癌诊疗指南》首次纳入免疫治疗为推荐疗法,以纳武利尤单抗为代表的PD-1单抗成为MSI-H/dMMR结直肠癌一线、二线及以上的治疗新选择。
指南推荐主要基于Checkmate-142研究的数据。结果显示,纳武利尤单抗单药队列在MSI-H/dMMR结直肠癌患者的后线治疗中具有显著优势,ORR为34%;而纳武利尤单抗联合低剂量伊匹木单抗队列的中期分析数据表明,联合方案ORR较单药治疗提高超1.5倍至58%,1年OS率更达85%,体现出令人振奋的有效性。
而根据2018年ESMO大会首次报道的Checkmate-142研究中MSI-H/dMMR结直肠癌患者接受一线联合免疫治疗数据,45例患者接受纳武利尤单抗联合超低剂量伊匹木单抗治疗,ORR为64%,DCR为84%,1年PFS率与OS率分别为77%与84%。对比过往非一线数据,此项一线数据明显优于后线单药与联合治疗的ORR,这提示免疫治疗越先使用,其有效率可能会越高。当然,一线临床应用的有效性与安全性还需要更长随访时间以及更大样本量来给我们确切的答案。
▼
纳武利尤单抗在胃癌与结直肠癌治疗中取得的突破性进展,已然掀起了免疫治疗应用于胃肠道肿瘤领域的热潮。相信在不久的将来,以纳武利尤单抗为代表的肿瘤免疫治疗能为中国胃肠道肿瘤患者带来更多生存获益。
*目前,纳武利尤单抗尚未在中国获批胃癌以及结直肠癌适应证。
参考文献
[1] Lancet. 2017 Dec 2;390(10111):2461-2471. doi: 10.1016/S0140-6736(17)31827-5. Epub 2017 Oct 6.
[2] SATOH T, CHEN L T, KANG Y K, et al. phase III study of nivolumab (nivo) in previously treated advanced gastric or gastric esophageal junction (G/GEJ) cancer (ATTRACTION-2): Two-years update data[R]. 2018 ESMO Abstract 617PD.
[3] Chao Y, Chen JS, Yeh KH, et al. Nivolumab in Advanced Gastric or Gastroesophageal Junction Cancer Refractory to, or Intolerant of, at Least Two Previous Chemotherapy Regimens: a Taiwaness Subgroup Analysis of ATTRACTION-2 Study. GEST (2019) Annual Meeting.
[4] WHO: International Agency for Research on Cancer, Stomach, Globocan, 2018
[5] Jihyung Hong, Yiling Tsai, et al. The economic burden of advanced gastric cancer in Taiwan. BMC Health Serv Res. 2017; 17: 663.
[6] 季加孚. 我国胃癌防治研究三十年回顾 [J]. 中国肿瘤临床,2013,40(22)
[7] Venderbosch S, Nagtegaal ID, Maughan TS, et al. Mismatch repair status and BRAF mutation status in metastatic colorectal cancer patients: a pooled analysis of the CAIRO, CAIRO2, COIN, and FOCUS studies. ClinCancer Res 2014;20:5322-5330.
[8] Lancet Oncol. 2017 Sep;18(9):1182-1191. doi: 10.1016/S1470-2045(17)30422-9. Epub 2017 Jul 19.
[9] André, et al. ASCO 2017.
[10] H.J. Lenz, E. van Cutsem, M.L. Limon, et al. ESMO 2018.


























